一、EC 62304與YY/T 0664的核心定位與關系
IEC 62304(IEC 62304)是國際通用的醫療器械軟件生命周期管理標準,適用于所有包含軟件的醫療器械(如嵌入式軟件、獨立軟件、移動應用等),其核心目標是確保軟件的安全性、可靠性和合規性。標準將軟件安全等級分為A/B/C三級(對應無傷害/非嚴重傷害/死亡或嚴重傷害的可能性),并要求根據等級實施差異化的開發、驗證和風險管理流程。
YY/T 0664是中國等同采用IEC 62304的國家醫藥行業標準,于2020年更新(替代2008版),進一步結合中國醫療器械監管要求。其適用范圍與IEC 62304一致,但強化了網絡安全、數據完整性等本土化要求。
二、核心框架與生命周期管理對比
1. EC 62304的核心要求:?
- 軟件安全分類:根據潛在風險劃分A/B/C類,例如血糖儀嵌入式軟件若錯誤可能導致低血糖昏迷則歸為C類,需最高級別控制。
- 風險管理整合:需與ISO 14971結合,建立故障樹分析(FTA)和失效模式與影響分析(FMEA),覆蓋從需求分析到退役的全周期風險控制。
- 驗證與確認:要求通過單元測試、集成測試、系統測試及可追溯性矩陣(RTM)確保需求覆蓋。
2. YY/T 0664的特殊性:?
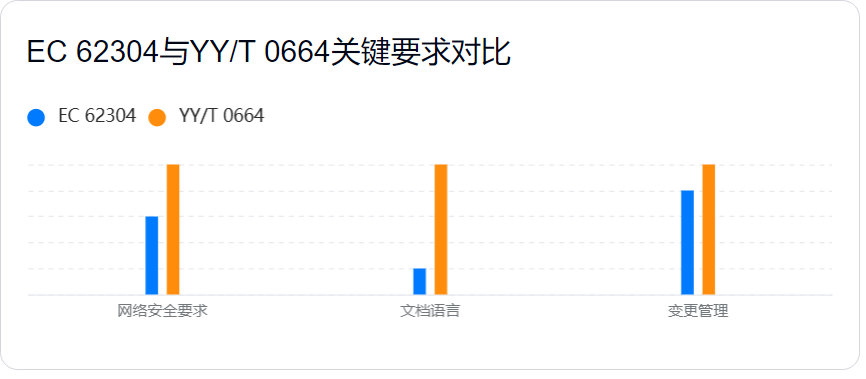
- 網絡安全要求:明確要求對數據加密、訪問控制、漏洞管理進行驗證(如心電圖軟件需防范數據篡改)。
- 文檔本地化:開發文檔需符合中國《醫療器械軟件注冊技術審查指導原則》,例如需提交軟件需求規格書(SRS)和軟件維護計劃的簡體中文版本。
三、關鍵流程差異與實施難點
| 對比維度 | IEC 62304 | YY/T 0664 |
|---|---|---|
| 適用對象 | 全球市場(歐盟CE、美國FDA等認可) | 中國市場(NMPA強制要求) |
| 網絡安全要求 | 一般性要求(如IEC 82304補充) | 明確要求符合GB/T 37061-2018等國家標準 |
| 文檔語言 | 接受多語言版本 | 需提供中文技術文檔 |
| 變更管理 | 強調變更影響分析 | 額外要求向藥監部門報告重大軟件更新(如算法核心邏輯修改)? |
四、實際應用中的協同與挑戰
1. 協同點:
- 兩者均要求建立軟件開發生命周期(SDLC),覆蓋需求分析、設計、編碼、測試、部署和維護階段,且需通過配置管理工具(如Git、SVN)追蹤版本變更。
2. 挑戰:
- 雙重合規成本:出口企業需同時滿足EC 62304的追溯性審計和YY/T 0664的網絡安全測試(如滲透測試)。
- 獨立軟件的特殊性:YY/T 0664對獨立軟件(如AI輔助診斷系統)要求更嚴格,需額外提供臨床評價報告,而IEC 62304依賴第三方標準(如IEC 82304-1)補充
`函數)
![[創業之路-364]:穿透表象:企業投資的深層邏輯與誤區規避](http://pic.xiahunao.cn/[創業之路-364]:穿透表象:企業投資的深層邏輯與誤區規避)

![[實戰] 天線陣列波束成形原理詳解與仿真實戰(完整代碼)](http://pic.xiahunao.cn/[實戰] 天線陣列波束成形原理詳解與仿真實戰(完整代碼))















——CADc#實現)