今天給同學們分享一篇實驗文章“Oral mucosal breaks trigger anti-citrullinated bacterial and human protein antibody responses in rheumatoid arthritis”,這篇文章發表在Sci Transl Med期刊上,影響因子為17.1。

結果解讀:
口腔黏膜破裂會引發全身性炎癥反應
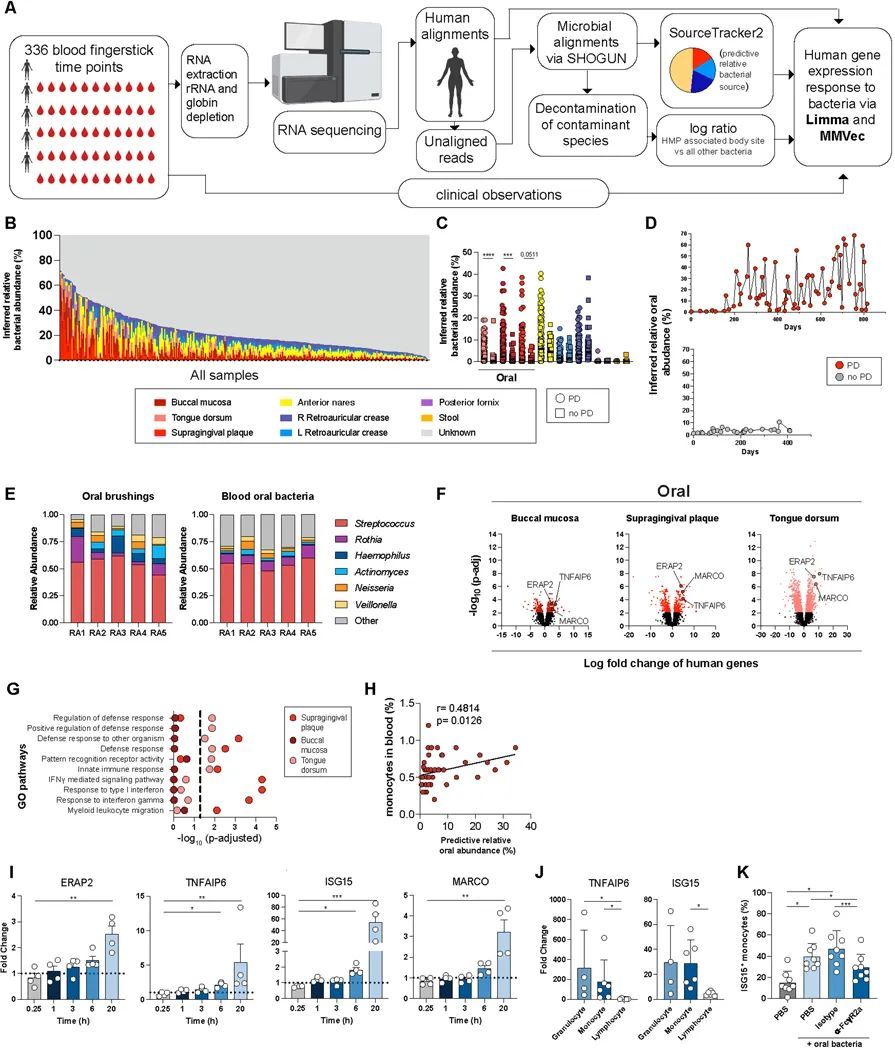
為了確定微生物組在患有牙周病的類風濕關節炎患者中的作用,作者對RA患者的血液樣本進行了批量RNA測序(RNA-Seq)分析,其中包括患有牙周病和未患牙周病的患者,樣本是通過每周一次的指尖采血,在一到四年的時間內獲得的(洛克菲勒大學縱向隊列,五名患者,每名患者平均n=67個時間點)。首先將RNA-Seq轉錄本與人類基因組(hg38)進行比對,以進行差異基因表達分析。然后將去除人類轉錄本的讀取結果與微生物宏基因組數據庫(Web of Life, WoL)進行比對(21),隨后進行了一個體外去污染流程(22)(圖1A-B)。為了確定血液中細菌的粘膜來源,作者使用SourceTracker2(23)推斷了來自三個口腔粘膜部位(頰粘膜、牙齦上方菌斑和舌背)以及其他五個身體部位(糞便、陰道穹窿、鼻前庭、左右耳后襞)的細菌相對豐度,并使用人類微生物組計劃(HMP)的相應身體部位樣本進行了匹配(24)。由于HMP數據集沒有使用轉錄組學,作者通過將該流程應用于公開可用的人類糞便樣本的轉錄組數據集(25)來驗證該方法。作者確定幾乎所有預測的身體部位都是糞便。
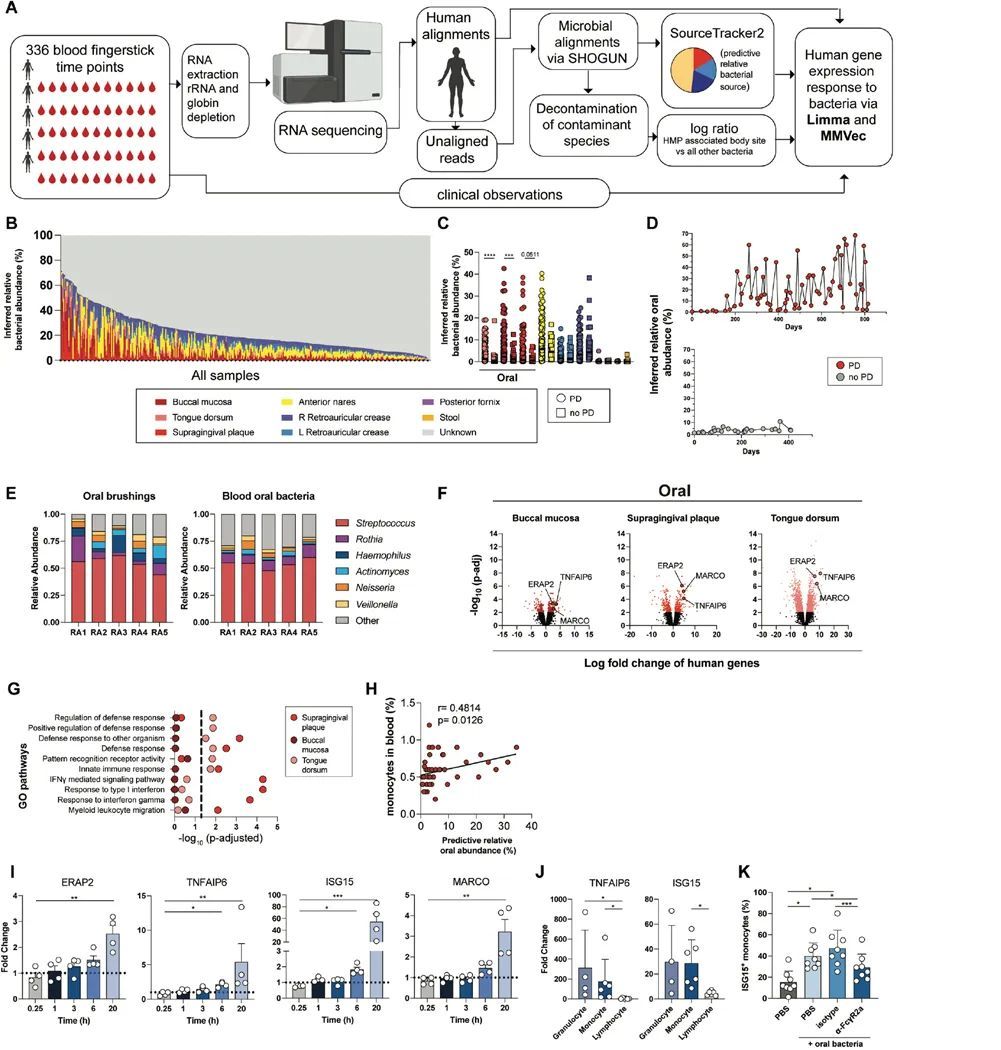
在類風濕關節炎發作期間和口腔細菌血癥反應中,炎癥滑膜單核細胞基因在血液中富集
作者接下來的目標是確定牙周病患有關的口腔細菌血癥是否會導致類風濕關節炎的急性發作。在作者之前的類風濕關節炎急性發作研究中(28),作者發現與基線相比,血液中的髓系相關途徑在急性發作期間得到了豐富。使用圖1中的同一縱向隊列,作者比較了急性發作期間的基因表達與基線,并確定了牙周病患和非牙周病患的類風濕關節炎患者的差異表達基因(圖2A)。作者將在牙周病關聯和非牙周病關聯的急性發作中具有一致折疊變化方向的基因分類為“共同發作基因”。相反,作者將在牙周病關聯和非牙周病關聯的急性發作中具有不一致折疊變化方向的基因分類為“牙周病特異性基因”(圖2B)。牙周病特異性發作基因,而不是共同發作基因,富集了髓系白細胞遷移、免疫復合物清除和免疫球蛋白結合(圖2C)。此外,只有牙周病特異性的爆發基因,而不是常見的爆發基因,富集了針對微生物和髓系免疫反應的抗體效應功能(圖2C)。綜上所述,這些數據表明:(i)對反復口腔細菌血癥的免疫反應有助于類風濕關節炎的爆發,(ii)口腔細菌血癥促進了患有牙周病的類風濕關節炎患者的抗體效應反應,以及(iii)對類風濕關節炎爆發的免疫特征是多變的,可能是由于不同的爆發觸發因素。

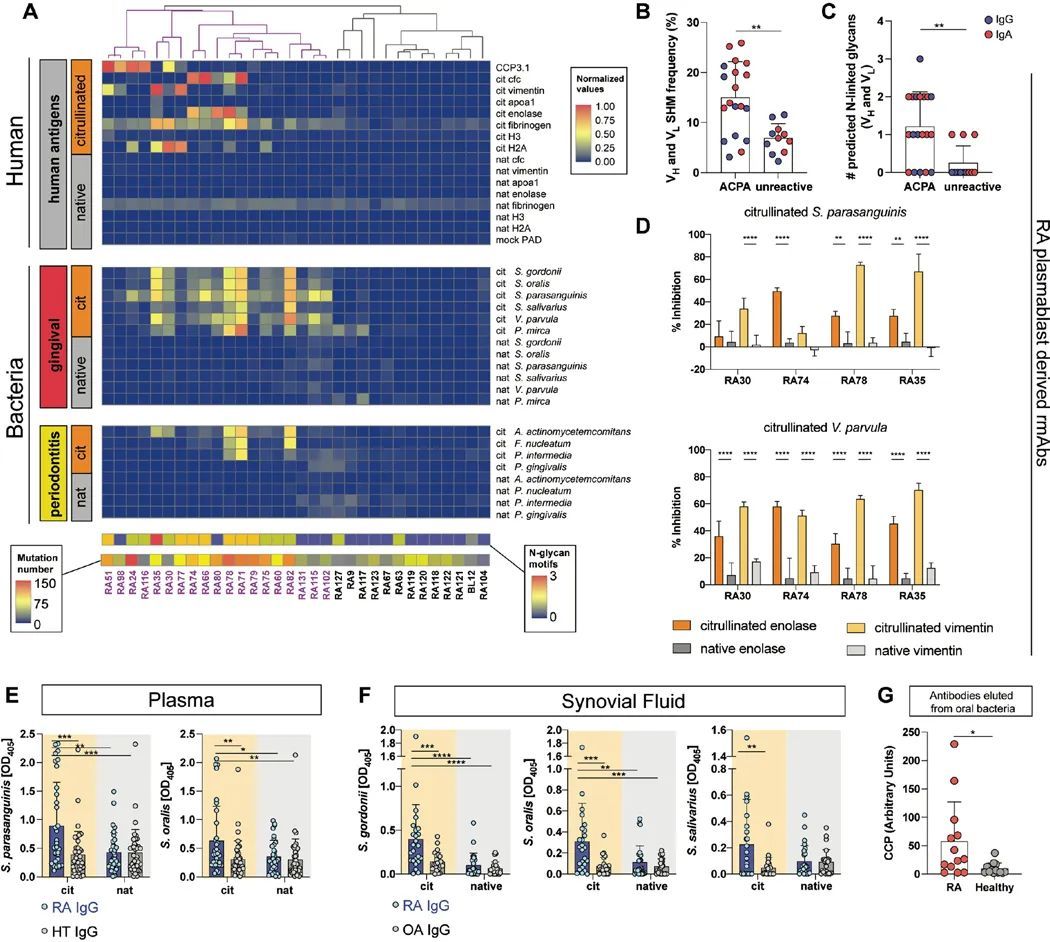
高度突變的RA抗體在體外結合了檸檬酸鹽化的人類和細菌抗原
作者推斷,如果患有牙周病的類風濕關節炎患者的發作與抗體效應功能有關,那么相對于沒有類風濕關節炎的個體,類風濕關節炎患者可能會對口腔細菌產生額外的、更具特異性的反應。鑒于牙周病特別與抗環瓜氨酸蛋白抗體(ACPA)相關(31),作者假設ACPA可能與口腔細菌發生交叉反應。因此,作者對源自人類類風濕關節炎血漿細胞母細胞的單克隆抗體進行了篩選,針對一系列與口腔粘膜以及其他粘膜部位特征相關的人類蛋白和細菌裂解物。與人類瓜氨酸化自身抗原結合的類風濕關節炎單克隆抗體(ACPA單克隆抗體)與一系列體外瓜氨酸化細菌裂解物發生交叉反應,但與天然細菌裂解物或體外瓜氨酸化所用的PAD酶沒有反應(圖3A),表明它們也是抗瓜氨酸化細菌抗體(ACBA)。沒有特異性針對瓜氨酸化人類抗原的類風濕關節炎抗體(非反應性單克隆抗體)對任何細菌裂解物的反應性很小(圖3A)。值得注意的是,ACPA和不活化的mAb之間在B細胞受體(BCR)特征方面沒有差異,如CDR3長度或親水性(GRAVY分數)。相反,與不活化的mAb相比,ACPA mAb在重鏈和輕鏈(V H 和V L )基因的V區域中攜帶更多的體細胞高度突變(SHM)(圖3B),后者與其他臨床情況下的抗體反應具有相似的SHM百分比(32, 33)。此外,作者還調查了抗原結合片段(Fab)區域中N-連接糖基化基序(由一致序列N-X-S/T(34)定義),這些基序是促進與細菌凝集素結合的糖基化位點(19)。ACPA mAb含有預測的N-連接糖基化基序數量增加(圖3C),與先前的報告一致(16, 35)。
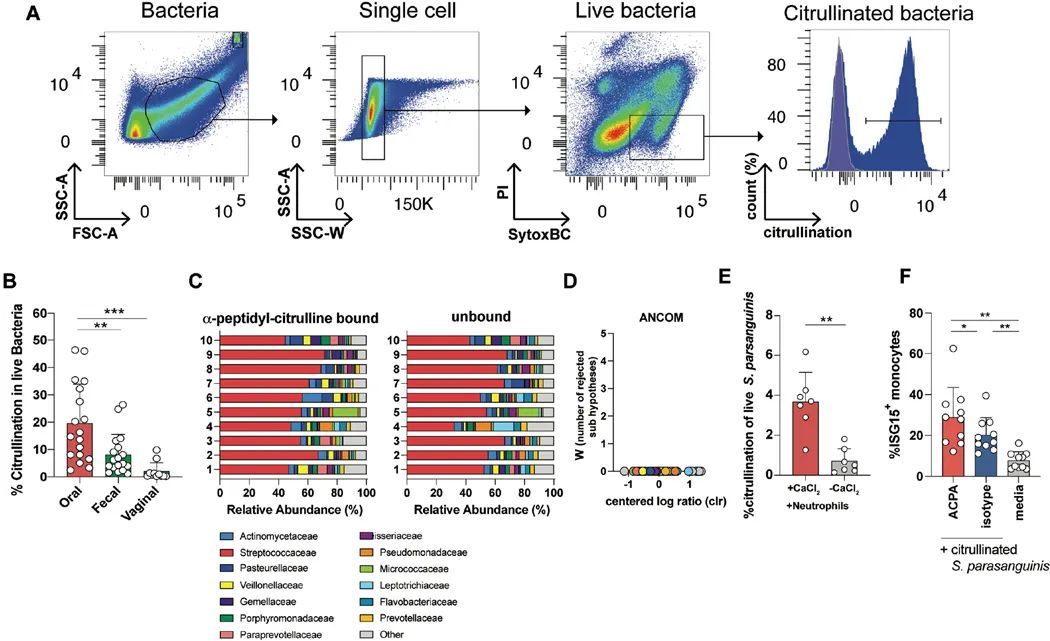
口腔細菌在體內高度脫氨酸化
作者接下來測試了各種黏膜部位的細菌在體內的脫氨酶作用程度。通過流式細胞術使用抗脫氨酶肽抗體分析了來自口腔、糞便和陰道的細菌的脫氨酶作用(圖4A)。與糞便和陰道細菌相比,口腔細菌的脫氨酶作用比例最高(圖4A,B)。
RA ACPA在體內結合到通過質譜檢測到的脫氨基酸化細菌肽上
為了確定體內某些細菌的檸檬酸化表位,作者分析了一個包含30個人類唾液樣本(43)的公開質譜數據集,這些樣本來自牙周病患者、健康個體和齲齒患者,并鑒定出了五個含有去甲基化精氨酸的細菌源性肽段(圖5A)。然后,作者測試了作者的21種抗胞核抗體(ACPA mAbs)庫,以確定其是否與質譜檢測到的這五個檸檬酸化細菌表位結合。其中八種ACPA mAbs與一個或多個檸檬酸化細菌表位強烈反應,表明人類唾液中存在的檸檬酸化細菌表位也被ACPA所識別(圖5B)。
總結
總之,本文所述的研究結果表明,牙周病通過反復的粘膜破裂,導致復發的先天性和適應性免疫激活,這可能有助于RA的發病機制。作者的研究結果表明,未來需要進行研究,以確定改善口腔護理是否可以在RA的管理中提供治療益處。












![[java學習日記]反射、動態代理](http://pic.xiahunao.cn/[java學習日記]反射、動態代理)
操作 Excel 詳解)



ServerBootstrap)

